Émulation d’essais cibles pour évaluer la durée optimale de traitement par inhibiteurs de points de contrôle immunitaire des mélanomes avancés
Contexte : Les inhibiteurs de points de contrôle immunitaire (immune checkpoint inhibitors, ICI) ont démontré leur efficacité pour les mélanomes de stade avancé, avec une survie globale à 7,5 ans proche de 50 %. Les essais cliniques prévoyaient un traitement jusqu’à progression ou toxicité, ou pour une durée maximale de deux ans. Le suivi après l’arrêt du traitement des patients répondeurs montre une réponse maintenue et un faible risque de rechute dans les mois qui suivent l’arrêt. À ce jour, la durée optimale du traitement anti-PD-1 pour le mélanome métastatique n’est cependant toujours pas établie. L’objectif de ce travail était d’évaluer la durée optimale de l’administration d’ICI.
Méthodes : Nous avons émulé des essais cibles en utilisant une approche par clonage, pondération et censure (cloning, censoring and weighting). Chaque émulation d’essai cible visait à comparer l’effet de l’arrêt ou de la poursuite des ICI à un moment précis, parmi les patients encore sous traitement et dont la maladie était contrôlée à ce moment-là. Les données des patients inclus dans la cohorte MelBase entre 2015 et 2021 ont été utilisées.
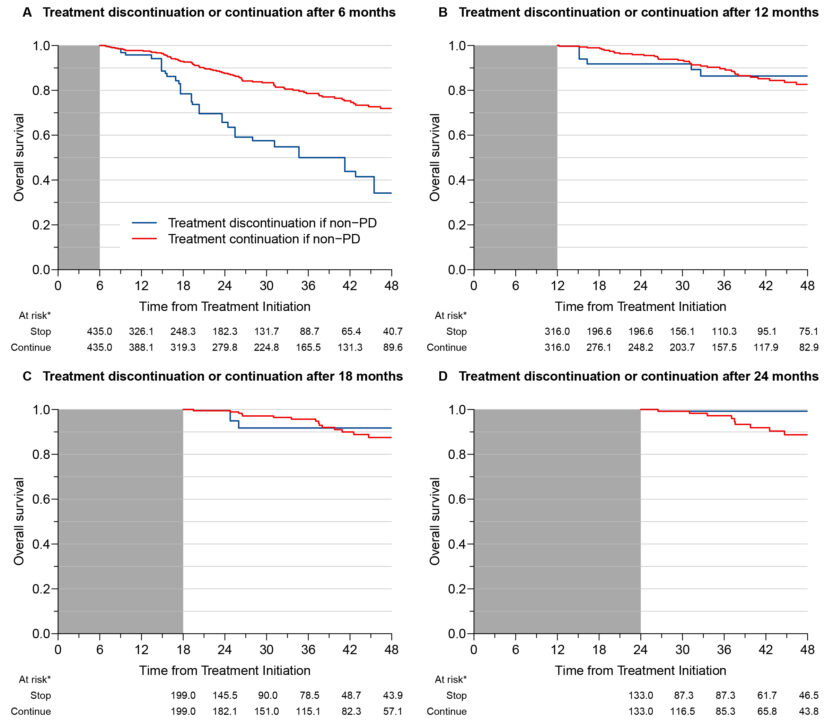
Résultats : 435 participants de la cohorte MelBase étaient éligibles et ont été inclus dans l’essai émulé d’interruption de traitement à 6 mois. Les résultats ont montré une survie globale significativement plus faible lorsque le traitement a été interrompu que lorsqu’il a été prolongé pendant au moins trois mois. La différence de survie à 48 mois était de 37,8 % (intervalle de confiance à 95 % [IC] 19,8-60,5), et la différence de durée de survie moyenne restreinte correspondante était de 8,3 mois (IC à 95 % : 4,1-12,7). Ni l’essai émulé sur l’arrêt du traitement à 12 mois ni celui sur l’arrêt du traitement à 18 mois n’ont mis en évidence un avantage de l’arrêt ou de la poursuite du traitement par ICI à l’un ou l’autre de ces moments. Les résultats de l’essai émulé d’interruption du traitement à 24 mois étaient plus favorables à l’interruption qu’à la poursuite du traitement à ce stade, avec un taux de survie absolu à 48 mois supérieur de 10,5 % (IC à 95 % : 4,4-18,1).
Interprétation : Ces résultats suggèrent qu’une immunothérapie d’un an est à la fois nécessaire et vraisemblablement suffisante pour les patients atteints de mélanome avancé dont la maladie est contrôlée. Un traitement prolongé au-delà de 2 ans ne semble pas être bénéfique en termes de survie et pourrait même être préjudiciable.
Par Raphaël Porcher